
Pesquisa
Nos primeiros meses de execução do Projeto, as metodologias a serem utilizadas para isolamento, identificação das BRAs, sequenciamento do genoma completo de BRAs selecionadas e análise metagenômica serão testadas, validadas e padronizadas. Os laboratórios da Rede (que poderão ser Laboratórios Centrais de Saúde Pública – LACEN, Instituto Evandro Chagas (IEC), CETESB, da Rede Genômica da Fiocruz ou laboratórios das universidades participantes, a depender da cidade), terão seus profissionais capacitados para realização das análises. Com apoio dos Prestadores de Serviços de Saneamento (PSS) locais (parceiros do projeto) serão definidos os pontos de amostragem e elaborados protocolos para a coleta e transporte das amostras até o laboratório.
Plano de Monitoramento
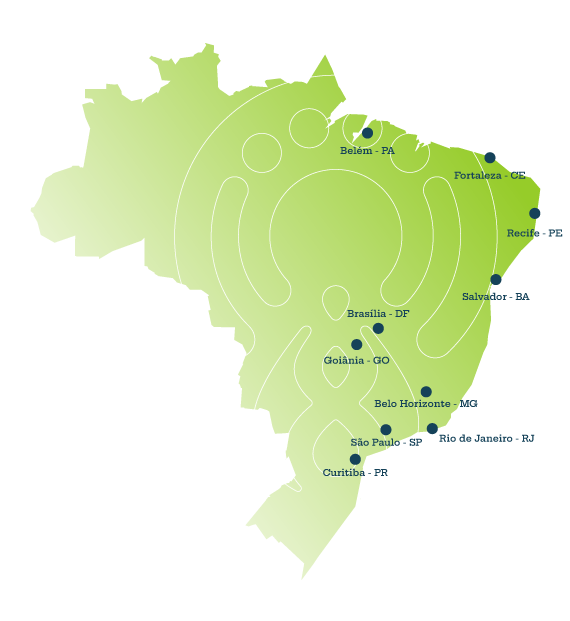
As amostras serão coletadas no esgoto bruto (afluente) em duas ETEs de cada cidade integrante da Rede de Pesquisa, sendo contemplada ao menos uma cidade em todas as regiões do país (Norte, Nordeste, Centro Oeste, Sul e Sudeste). O esgoto gerado em um hospital de referência no tratamento de doenças infecciosas de cada cidade também será coletado e monitorado. As cidades a serem contempladas no plano de monitoramento são listadas na figura.
Coleta, preservação e transporte das amostras
Para a coleta das amostras, a Rede de Pesquisa ReViRAE contará com o apoio dos Prestadores de Serviços de Saneamento (PSS) locais, estes serão responsáveis, também, pelo transporte das amostras até os laboratórios cadastrados no projeto (LACEN ou UNIVERSIDADE).
O esgoto de cada ponto de amostragem será coletado por meio de amostragem composta, utilizando amostrador automático. A coleta composta terá duração de 24 horas nas ETEs, para a amostragem do esgoto dos hospitais o tempo de coleta será definido pelos parceiros. As amostras serão mantidas à temperatura entre 4°C e 8°C durante todo o período da coleta e transporte até os laboratórios para subsequente realização das análises.
As coletas serão realizadas com frequência mensal para isolamento e identificação das BRAs. O sequenciamento do genoma completo será realizado para as cepas de maior relevância, com base na avaliação da RAM fenotípica.
Para as análises metagenômicas, serão realizadas seis campanhas amostrais, ou seja, a cada dois meses.
Cultivo e identificação de BRAs e construção do
resistoma a partir do sequenciamento genômico
completo
A etapa de isolamento e identificação das BRAsserá realizada nos Laboratórios Centrais de Saúde Pública (LACEN) ou em laboratórios de apoio das Universidades Federais, a depender da cidade monitorada. O sequenciamento genômico completo de BRAs será realizado em laboratório da Coordenação de Vigilância Genômica da FIOCRUZ/RJ.
Para o isolamento de K. pneumoniae e E. coli será utilizada a técnica de concentração por membrana filtrante (42 mm por 142 mm de diâmetro, com porosidade de 0,45 µm). Estas membranas serão depositadas em meios de cultivo seletivos e diferenciais, meio KPC para isolamento/diferenciação de K. pneumoniae spp e ESBL para E. coli.
Após período de incubação, serão selecionadas até 5 colônias para repique em ágar nutriente com o intuito de promover o isolamento adequado das cepas. As colônias de Escherichia coli em meio ESBL são, normalmente, de coloração roxa, enquanto as colônias de Klebsiella pneumoniae em meio KPC possuem coloração verde. A coloração das colônias não é característica exclusiva dessas espécies bacterianas, entretanto, a coloração inicial já é uma forma de seleção das bactérias alvo.
Quando a cepa já estiver bem isolada, com aspecto morfológico homogêneo em toda placa, a mesma já pode ser enviada para detecção pelo MALDI-ToF em placas de Petri. As placas devem apresentar colônias isoladas, novas, com tempo de incubação próximo ao ideal para o crescimento dos micro-organismos. No caso de E. coli e K. pneumoniae, esse tempo seria de 24 horas.
As cepas isoladas e identificadas serão avaliadas quanto ao seu perfil de suscetibilidade antimicrobiana frente a um painel de drogas antimicrobianas de relevância sob o ponto de vista humano e àqueles preconizados pela Organização Mundial de Saúde (OMS), pelo método automatizado Vitek-2®. Os resultados serão interpretados de acordo com o BrCAST/EUCAST (Ano vigente), com controle de qualidade realizada através de MIC conforme orientação ditada nos guidelines acima especificados.
As cepas que apresentarem o perfil MDR (multirresistência para drogas de última geração/ Cefalosporinas de 3ª/4ª geração, Carbapenens e Fluoroquinolonas) serão submetidas ao sequenciamento do genoma completo (Whole Genome Sequencing –WGS) pela plataforma Illumina, pelo sequenciador MiSeq, estas deverão ser enviadas para FIOCRUZ/RJ.
Metagenômica comparativa para avaliação de comunidades microbianas e monitoramento dos genes de resistência aos antimicrobianos (resistoma) no esgoto
Uma abordagem metodológica inovadora de sequenciamento NGS por enriquecimento e hibridização de alta densidade será empregada para a determinação sensível e específica de comunidades clinicamente relevantes, entre bactérias, vírus e fungos (280 patógenos), com investigação concomitante de um painel de >2.000 genes/alelos de RAM. Para cada um dos 10 centros participantes, serão criteriosamente selecionados 3 sítios e cujas amostras serão monitoradas bimestralmente durante 12 meses, totalizando até 6 pontos de seguimento e até 180 amostras para as análises de metagenômica. O processamento, sequenciamento e análises dessas amostras serão realizadas pela Rede de Vigilância Genômica da Fundação Oswaldo Cruz (Fiocruz), representadas nesta proposta pela Fiocruz-RJ e Fiocruz-CE e seus parceiros em 6 capitais (RJ, CE, BA, AM, PE e MG)
Identificação e quantificação de antimicrobianos
e seus metabólitos
Algumas amostras de esgoto serão selecionadas para identificação e quantificação de resíduos de antimicrobianos e seus metabólitos. Serão identificados por meio do estabelecimento de etapas de extração e pré-concentração, seguido da análise por cromatografia líquida acoplada à espectrometria de massas. Análises não-alvo (non-target) poderão ser implementadas para identificação de substâncias empregando-se sistemas de espectrometria de massas de alta-resolução, como Q-ToF, enquanto a quantificação de substâncias será realizada em sistemas do tipo triplo quadrupolo ou híbrido, quadrupolo/captura de íons.

Telefones
85 3025 9856 / 31 3059 7526
contato@revirae.com.br
copyright © Projeto ReVIRAE - 2024
